HIDROCARBONETOS
Hidrocarbonetos são
compostos formados exclusivamente de carbono e hidrogênio, que também
são chamados hidrocarburetos, carboidretos, carbetos, carburetos ou
carbonetos de hidrogênio.
Classificação e ocorrência
Os hidrocarbonetos se classificam de
acordo com a proporção dos átomos de carbono e hidrogênio presentes em
sua composição química. Assim, denominam-se hidrocarbonetos saturados
os compostos ricos em hidrogênio, enquanto os hidrocarbonetos ditos
insaturados apresentam uma razão hidrogênio/carbono inferior e são encontrados principalmente no petróleo e em resinas vegetais.
Os grupos de hidrocarbonetos
constituem as chamadas séries homólogas, em que cada termo (composto
orgânico) difere do anterior em um átomo de carbono e dois de
hidrogênio. Os termos superiores da série homóloga saturada, de peso
molecular mais alto, encontram-se em alguns tipos de petróleo e como
elementos constituintes do pinho, da casca de algumas frutas e dos
pigmentos das folhas e hortaliças.
Os hidrocarbonetos etilênicos,
primeiro subgrupo dos insaturados, estão presentes em muitas modalidades
de petróleo em estado natural, enquanto os acetilênicos, que compõem o
segundo subgrupo dos hidrocarbonetos insaturados, obtêm-se
artificialmente pelo processo de craqueamento (ruptura) catalítico do
petróleo. Os hidrocarbonetos aromáticos foram assim chamados por terem
sido obtidos inicialmente a partir de produtos naturais como resinas ou
bálsamos, e apresentarem odor característico. Com o tempo, outras
fontes desses compostos foram descobertas. Até a segunda guerra
mundial, por exemplo, sua fonte mais importante era o carvão. Com o
crescimento da demanda, durante e após a guerra, outras fontes foram
pesquisadas. Atualmente, grande parte dos compostos aromáticos, base de
inúmeros processos industriais, se obtém a partir do petróleo.
Estrutura e nomenclatura
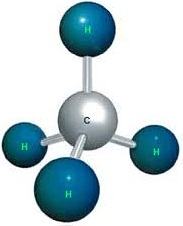
A estrutura das moléculas dos
hidrocarbonetos baseia-se na tetravalência do carbono, isto é, em sua
capacidade de ligar-se, quimicamente, a quatro outros átomos, inclusive
de carbono, simultaneamente. Assim, as sucessões de átomos de carbono
podem formar cadeias lineares, ramificadas em ziguezague, que lembram
anéis e estruturas de três dimensões.
Hidrocarbonetos saturados
A fórmula empírica molecular dos hidrocarbonetos saturados, também chamados alcanos ou parafinas, é CnH2n+2,
segundo a qual n átomos de carbono combinam-se com 2n + 2 átomos de
hidrogênio para formarem uma molécula. Valores inteiros sucessivos de n
dão origem aos termos distintos da série: metano (CH4), etano (C2H6), propano (C3H8), butano (C4H10) etc.
A partir do quarto termo da série, o
butano, os quatro carbonos podem formar uma cadeia linear ou uma
estrutura ramificada. No primeiro caso, o composto se denomina n-butano.
Na estrutura ramificada, um átomo de carbono se liga ao carbono
central da cadeia linear formada pelos outros três, formando o
iso-butano, ou pode dar origem a uma estrutura cíclica, própria do
composto chamado ciclobutano, em que os átomos de carbono das
extremidades estão ligados entre si. A existência de compostos com
mesma fórmula molecular, mas com estruturas diferentes, é fenômeno
comum nos hidrocarbonetos, designado como isomeria
estrutural. As substâncias isômeras possuem propriedades físicas e
químicas semelhantes, mas não idênticas, e formam, em certos casos,
moléculas completamente diferentes.
Os termos da série saturada são
nomeados a partir do butano com o prefixo grego correspondente ao número
de átomos de carbono constituintes da molécula: penta, hexa, hepta
etc., acrescidos da terminação "ano". Nos cicloalcanos, hidrocarbonetos
de cadeia saturada com estrutura em anel, a nomenclatura faz-se com a
anteposição da palavra "ciclo" ao nome correspondente ao hidrocarboneto
análogo na cadeia linear. Finalmente, os possíveis isômeros presentes
na série saturada cíclica se distinguem por meio de números, associados
à posição da ramificação no ciclo.
Exemlpo:
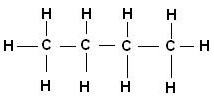
Butano
Hidrocarbonetos insaturados
O primeiro grupo de hidrocarbonetos
insaturados, constituído pelos compostos etilênicos, também chamados
alcenos, alquenos ou olefinas, tem como característica estrutural a
presença de uma dupla ligação entre dois átomos de carbono. Sua fórmula
molecular é CnH2n e os primeiros termos da série homóloga correspondente recebem o nome de etileno ou eteno (C2H4), propileno ou propeno (C3H6), butileno ou buteno (C4H8) etc. Os termos seguintes têm uma nomenclatura análoga à dos hidrocarbonetos saturados, acrescidos da terminação "eno".
A posição da dupla ligação na
molécula dos alcenos pode dar origem a diferentes isômeros. Para
distingui-los, o número do primeiro carbono a conter essa ligação
precede o nome do hidrocarboneto na nomenclatura desses compostos.
Existem, ainda, hidrocarbonetos etilênicos com mais de uma dupla ligação
-- denominados dienos, quando possuem duas ligações, e polienos, com
três ou mais. O grupo mais importante dessa classe de hidrocarbonetos
constitui-se de compostos com duplas ligações em posições alternadas, os
dienos conjugados. A nomenclatura dos alcenos de estrutura anelar,
ditos cicloalquenos, é formalmente análoga à dos cicloalcanos.
Os alcinos ou alquinos (de fórmula molecular CnH2n-2),
também conhecidos como hidrocarbonetos acetilênicos e componentes do
segundo grupo dos compostos insaturados, apresentam ligação tripla em
sua estrutura e sua nomenclatura é similar à dos alcenos, com a
terminação "ino" que lhes é própria. Os cicloalquinos inferiores (de
baixo peso molecular) são instáveis, sendo o ciclo-octino, com oito
átomos de carbono, o menor alcino cíclico estável conhecido.
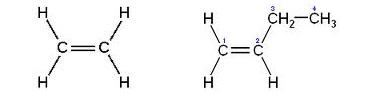
Exemplos:
Eteno Buteno
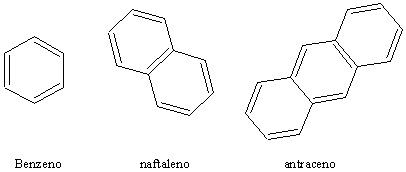
Hidrocarbonetos aromáticos
A estrutura do benzeno, base dos
hidrocarbonetos aromáticos, foi descrita pela primeira vez por Friedrich
August Kekulé, em 1865. Segundo ele, a molécula do benzeno tem o
formato de um hexágono regular com os vértices ocupados por átomos de
carbono ligados a um átomo de hidrogênio. Para satisfazer a
tetravalência do carbono, o anel benzênico apresenta três duplas
ligações alternadas e conjugadas entre si, o que lhe confere sua
estabilidade característica.
Os hidrocarbonetos da série homóloga
benzênica subdividem-se em três grupos distintos. O primeiro
constitui-se de compostos formados pela substituição de um ou mais
átomos de hidrogênio do anel pelos radicais de hidrocarbonetos. Esses
compostos têm seus nomes derivados do radical substituinte, terminado em
"il", e seguidos da palavra "benzeno". Alguns, no entanto, apresentam
denominações alternativas (ou vulgares), mais comumente empregadas.
Assim, o metil-benzeno é conhecido como tolueno, o dimetil-benzeno como
xileno etc.
No segundo grupo, encontram-se os
compostos formados pela união de anéis benzênicos por ligação simples
entre os átomos de carbono, como a bifenila, ou com um ou mais átomos de
carbono entre os anéis. Por último, o terceiro grupo de
hidrocarbonetos aromáticos constitui-se de compostos formados por
condensação de anéis benzênicos, de modo que dois ou mais átomos de
carbono sejam comuns a mais de um anel, tais como o naftaleno, com dois
anéis, e o antraceno, com três.
Exemplos:
Propriedades e aplicações
Os hidrocarbonetos em geral são
insolúveis em água, mas se solubilizam prontamente em substâncias
orgânicas como o éter e a acetona. Os primeiros termos das séries
homólogas são gasosos, enquanto os compostos de maior peso molecular são
líquidos ou sólidos. Graças a sua capacidade de decompor-se em dióxido
de carbono e vapor d'água, em presença de oxigênio, com desprendimento
de grande quantidade de energia, torna-se possível a utilização de
vários hidrocarbonetos como combustíveis.
Os hidrocarbonetos saturados, ou
parafinas, caracterizam-se sobretudo por ser quimicamente inertes.
Industrialmente, são empregados no processo de craqueamento (cracking)
ou ruptura, a elevadas temperaturas, e produzem misturas de compostos de
estruturas mais simples, saturados ou não. A hidrogenação catalítica
dos alcenos é utilizada, em escala industrial, para a produção
controlada de moléculas saturadas. Esses compostos são usados ainda como
moderadores nucleares e como combustíveis (gás de cozinha, em
automóveis etc.).
Os hidrocarbonetos insaturados com
duplas ligações têm a capacidade de realizar reações de adição com
compostos halogenados e formam importantes derivados orgânicos. Além
disso, com a adição de moléculas de alcenos, é possível efetuar a
síntese dos polímeros,
empregados industrialmente no fabrico de plásticos (polietileno,
teflon, poliestireno etc) e de fibras sintéticas para tecidos (orlon,
acrilan etc.). Além disso, faz parte da gasolina uma importante mistura
de alquenos. Metade da produção de acetileno é utilizada, como
oxiacetileno, na soldagem e corte de metais. Os hidrocarbonetos
aromáticos, além de bons solventes, são empregados na produção de
resinas, corantes, inseticidas, plastificantes e medicamentos.
©Encyclopaedia Britannica do Brasil Publicações Ltda
Autoria: Daniel Salomão Carvalho